- A+
1980年,人类就通过疫苗灭绝了天花病毒。自此,疫苗领域繁荣发展,乙肝、HPV、狂犬、百白破、乙脑等。
然而,癌症治疗性疫苗却进展缓慢,40年来一直很难有所突破……
直到今年初,编码最多34种新抗原的mRNA-4157癌症疫苗2b期临床试验公布了积极的结果,个体化新抗原癌症疫苗才得以获得大量关注!
癌症疫苗是如何发展的?mRNA-4157癌症疫苗意味着什么?人类能运用癌症疫苗来对抗癌症了吗?还有哪些难解决的因素?让我们一起走进本文!
个体化新抗原癌症疫苗的
发展一波三折
个体化癌症疫苗的主动特异性免疫治疗已经被研究了40多年, BioNTech联合创始人UgurSahin夫妇曾表示:“2030年左右,mRNA癌症疫苗可能上市。”
1.1 早期尝试:个体化癌症疫苗的疗效有限(1977年-2010年)
从20世纪70年代开始,研究者们就开始制作癌症疫苗,最初的成分是患者来源的自体肿瘤细胞或肿瘤裂解液,给患者注射后取得了一定的效果。
例如,Laucius和同事报告说,一种由辐照后自体黑色素瘤细胞和卡介菌佐剂混合的疫苗使得18名手术无法治愈的黑色素瘤患者中有4名转移消退。
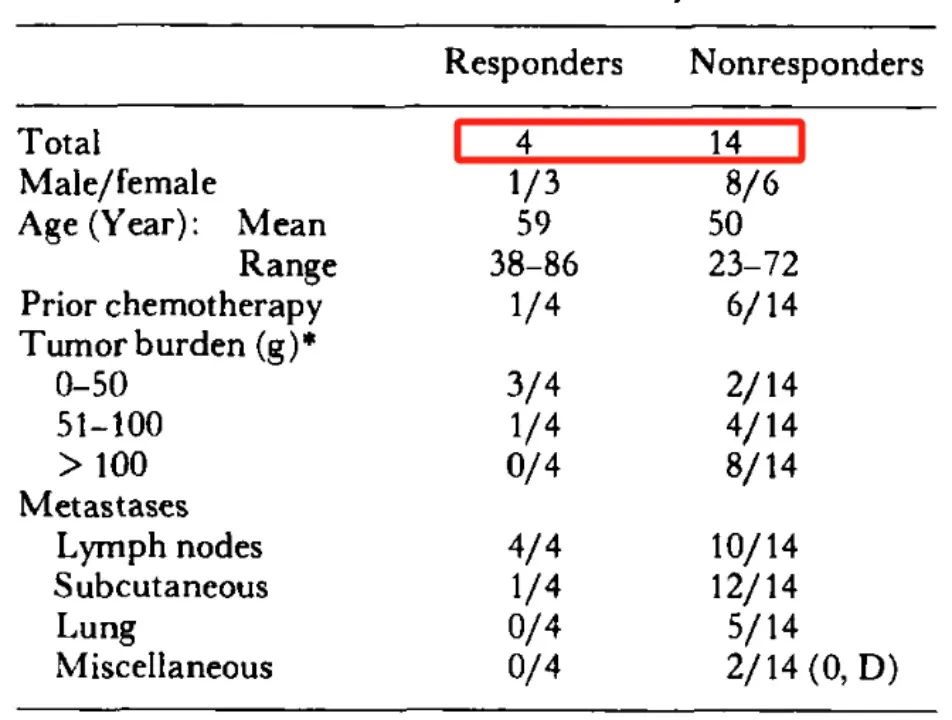
接着,来自美国费城的托马斯杰斐逊大学 (Thomas Jefferson University)的David Berd等人提出了新抗原的概念,指在肿瘤细胞中特异表达而正常组织中不存在的抗原。Berd等马上将这一概念进行实践验证,用半抗原二硝基苯基(DNP)修饰自体癌细胞,再将其回输入患者体内,以诱导患者自体免疫反应,消灭黑色素瘤癌细胞。III期临床显示,214位患者的5年生存率由手术的20%~25%提高至44%。
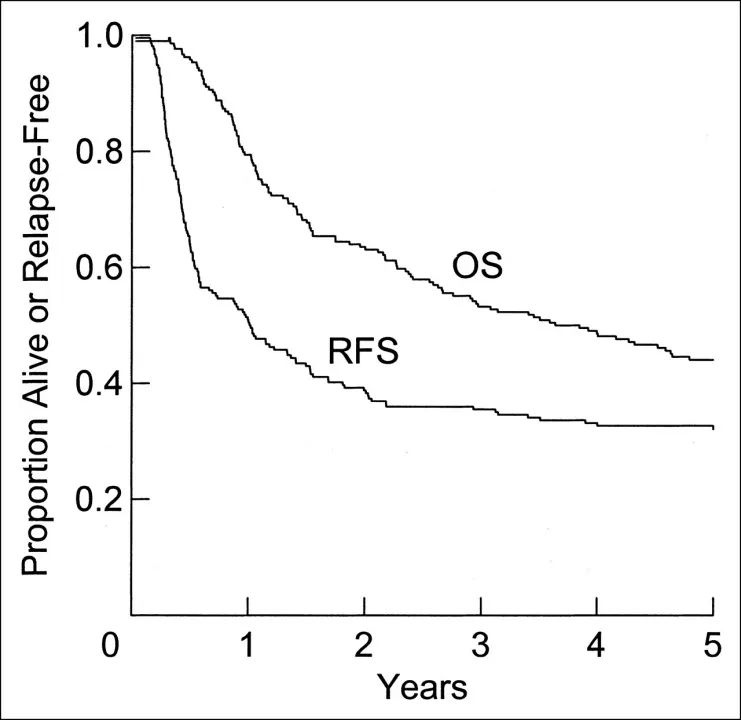
图1 五年无复发生存率(RFS)和总生存率(OS)是33%和44%
个体化癌症疫苗迎来最后的高潮。2010年,FDA首次批准了一款治疗性癌症疫苗用于晚期去雄抗性前列腺癌。该疫苗是一种自体树突状细胞疫苗,负载由前列腺酸性磷酸酶(pap)和粒细胞巨噬细胞集落刺激因子(gm-csf)构建的融合蛋白(pap-gm-csf)。
1.2 十年沉寂:免疫检查点的兴起(2011年-2022年)
然而,随着免疫检查点抑制剂(immune checkpoint inhibitors,ICIs)在过去的十年中陆续获得批准,癌症免疫治疗的重点从个体化癌症疫苗转移到非个体化治疗。ICIs治疗确实对少数癌症患者产生了长期的治疗效果,但仍然需要进一步提高疗效和尽量减少免疫相关毒性,这为后续的联合治疗埋下了伏笔。
1.3 强势崛起:mRNA疫苗实现临床突破!(2023年-至今)
最近,得益于对肿瘤表位免疫原性理解的进展和疫苗技术的改进,人们对所谓的基于新抗原的个体化癌症疫苗概念的兴趣被重新点燃。今年2月,《柳叶刀》报道了新型mRNA癌症疫苗(mRNA-4157)在美国和澳大利亚进行的多机构的2b期研究结果,与Pembrolizumab(PD-1抑制剂,ICIs)单药治疗相比,mRNA-4157治疗联合Pembrolizumab,显著延长了术后高危黑色素瘤患者的无复发生存期,并显示出可控的安全性。

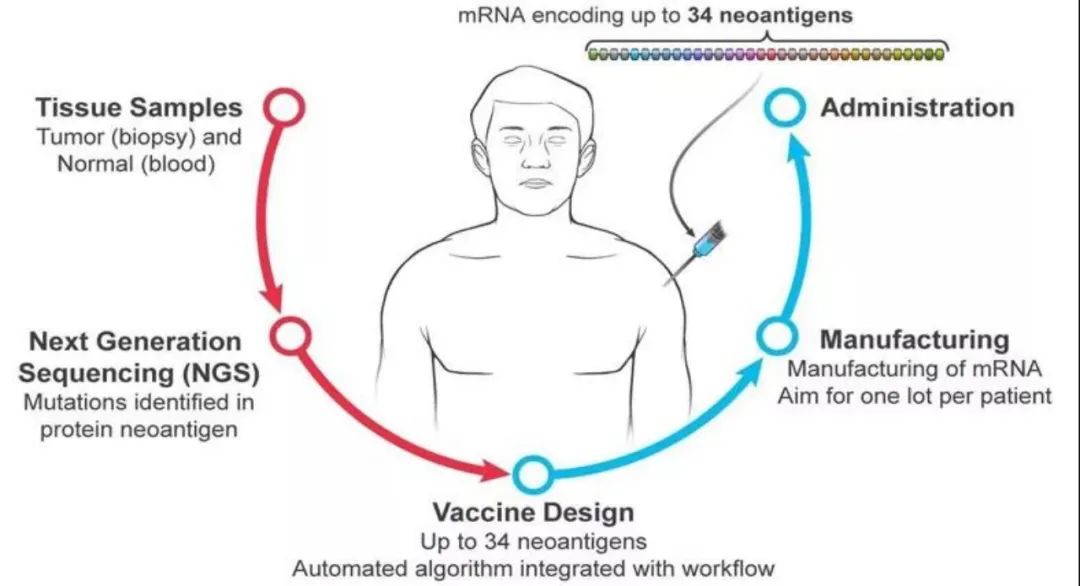
研究者对每个患者的肿瘤基因组进行了测序,并通过使用一种专有算法,建立了潜在的免疫原性肿瘤特异性新抗原。mRNA-4157疫苗是一种个体化的mRNA化合物,含有多达34种不同的患者特异性新抗原。单个疫苗的每个患者的最小目标表位数量为9个,91%的患者接受了编码完整34个表位的mRNA疫苗化合物。
根据一项开放标签的临床2b期试验——KEYNOTE-942/mRNA-4157-P201所得到的数据。157名患者(101名男性,56名女性)采用联合治疗(n=107)或单药治疗(n=50),平均随访23个月和24个月,该研究达到RFS主要终点,联合组可显著降低患者44%的复发或死亡风险。
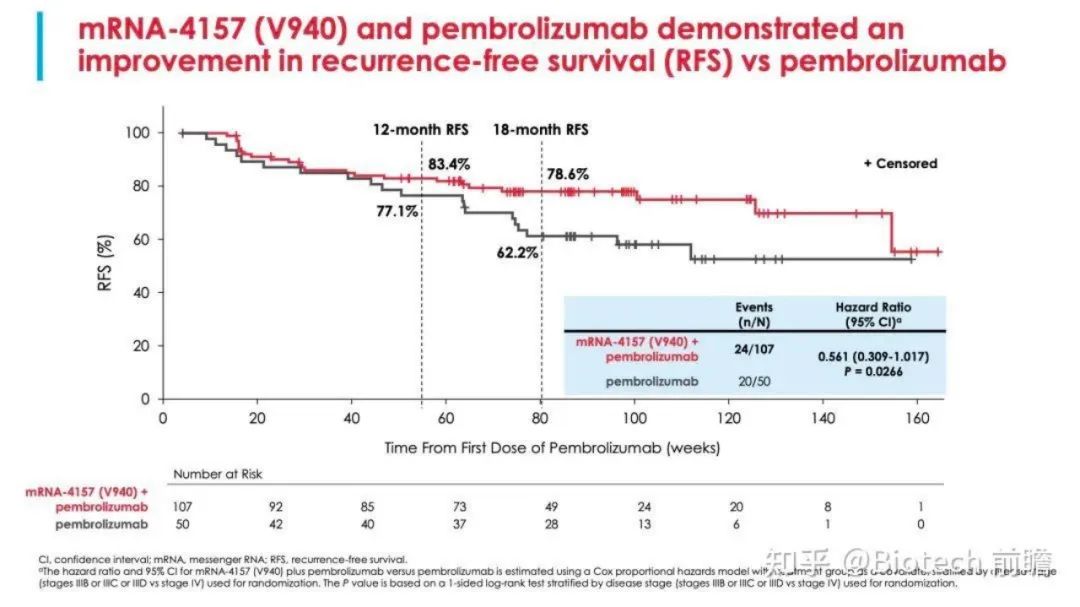
治疗相关不良事件多为1-2级。联合治疗组和单药治疗组分别有25%、18%患者发生了≥3级治疗相关不良事件,未发生与mRNA-4157相关4-5级事件。联合治疗组(37(36%))和单药治疗组(18 (36%))发生免疫介导不良事件的频率相似。
研制个体化新抗原癌症疫苗的主要技术
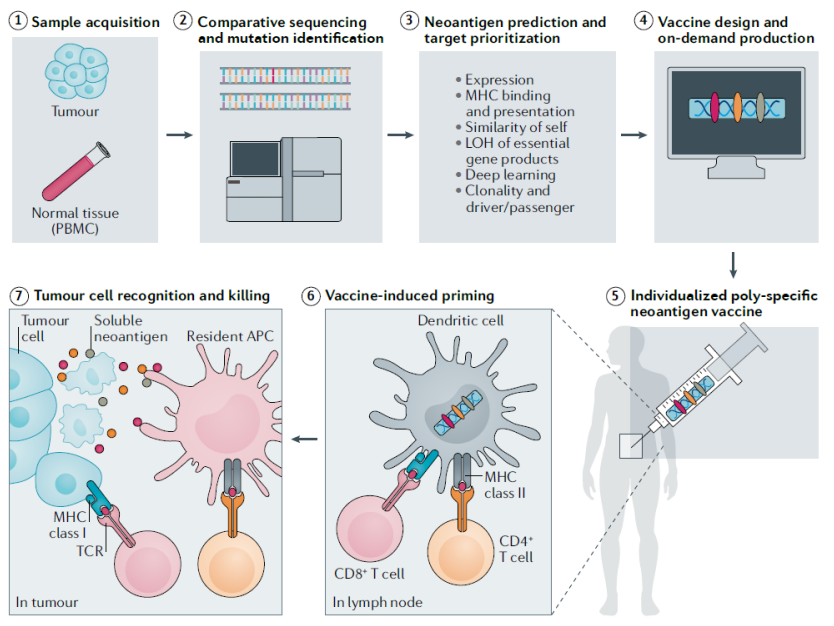
个体化新抗原癌症疫苗的制造过程是一个复杂且个体化的过程,发展到现在通常包括以下步骤:
①肿瘤样本采集:从患者体内获取肿瘤组织样本;
②基因组测序:对肿瘤样本进行基因组测序,以鉴定肿瘤细胞中的独特突变;
③新抗原预测和筛选:使用生物信息学工具和算法,分析基因组测序数据,预测可能产生的新抗原,对预测的新抗原进行筛选,选择最有可能引发强烈免疫应答的新抗原。
④疫苗设计和生产:根据筛选出的新抗原,设计个体化的癌症疫苗,包括选择合适的载体和佐剂,最后使用合适的生产技术,制造出个体化的新抗原癌症疫苗(DNA 疫苗,mRNA 疫苗,多肽/蛋白疫苗,细胞疫苗,工程化病毒/细菌疫苗)。
⑤质量控制:对生产的疫苗进行严格的质量控制,确保其安全性和有效性;
⑥患者接种:将疫苗接种到患者体内,激发免疫系统对肿瘤的攻击;
⑦监测与评估:对患者的免疫应答进行监测和评估,以了解疫苗的效果和安全性。
上述是一个大致的制造过程,实际情况可能会因不同的制造方法和技术而有所差异。
2.1 下一代测序技术是关键
得益于下一代测序技术(NGS)的进步以及成本降低等因素,使得在短时间内获得癌症患者的肿瘤突变信息变得相对容易,肿瘤新生抗原疗法也终于迈出了最关键的一步。
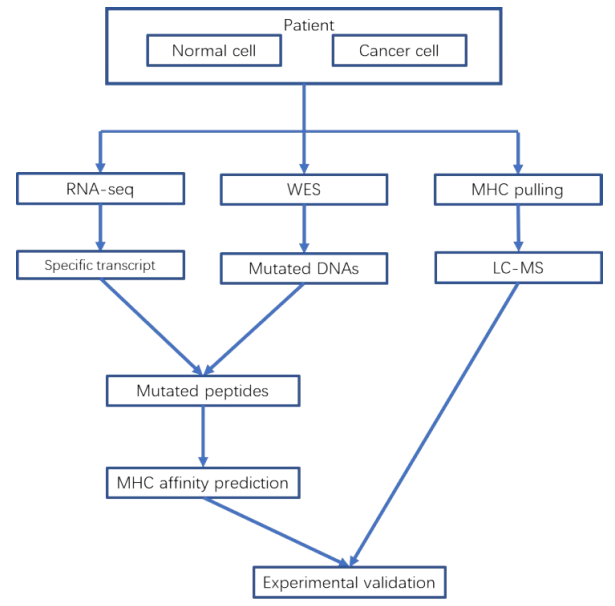
2.2 数字技术与人工智能/机器学习用于筛选新抗原
Moderna的算法能够基于人体外测定数据,高准确度的预测和筛选具有TIL反应性的新生抗原,mRNA-4157就是在此算法下诞生;BioNTech使用数字化的工具,进行新抗原的预测,以及新冠变种的监控与预测。
我们还有可能将AI模型应用于疫苗的设计工作以及递送方式改进。在疫苗靶点设计以及递送方式上利用人工智能对疫苗进行预测打分,从而大大减少前期筛选过程所耗费的时间和精力,而对设计结果的验证又会辅助提高模型的设计准确性,从而螺旋式提升疫苗的靶向性和有效性。
2.3 合成生物学加速实验研究并提高肿瘤疫苗在临床治疗效果
合成生物学方法贯穿整个疫苗研发流程,即利用中心法则与细胞免疫原理,通过人为改变某些步骤,加速新抗原识别与筛选,助力新疫苗的设计,诱使T细胞攻击肿瘤细胞以达到治疗目的。
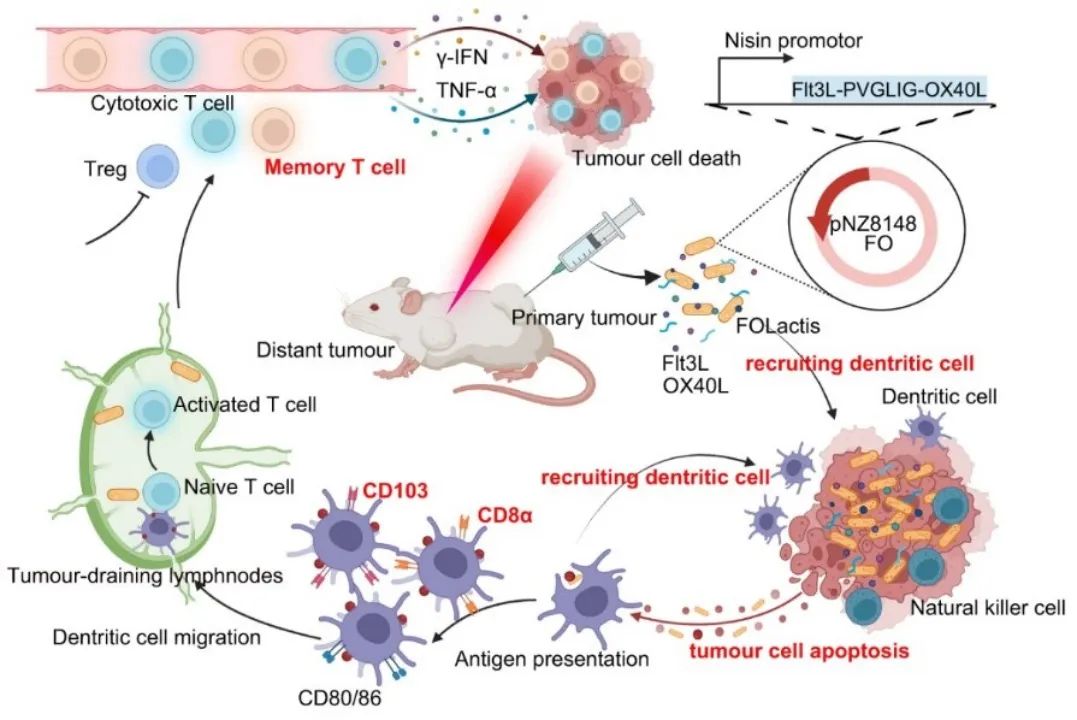
图6 FOLactis疫苗的全部合成流程
个体化新抗原癌症疫苗
复兴之下的危与机
3.1 危:关键问题仍然和40年前一样还未解决
虽然KEYNOTE-942临床研究中显示的数据向好,但其他基于新抗原的免疫疗法还未能显示出临床疗效。那么40年前在自体癌症疫苗时代就被讨论过的许多关键问题,如今我们又得再问一遍:
①需要靶向的最佳抗原是什么?是癌症驱动基因突变的定制化新抗原,独立基因突变的新抗原,还是通常检测到的驱动突变。
②疫苗产品的最佳佐剂是什么?是胞嘧啶-磷酸-鸟嘌呤寡脱氧核苷酸,IFN基因激动剂,还是用多聚赖氨酸和羧甲基纤维素稳定的聚肌苷-多胞苷酸?
③最佳的疫苗疗效方案是什么?剂量、途径、持续时间和时间(佐剂vs新佐剂)。
④哪种ICIs能最好地提高癌症疫苗的疗效?是CTLA-4、PD-1/PD-L1、还是LAG-3。
3.2 危:本身的技术挑战以及竞争产品压缩其生存空间
以新抗原为基础的癌症疫苗存在明显的两个技术挑战,一是选择已证实在肿瘤细胞的MHC凹槽上表达的免疫原性表位,二是为具有低肿瘤突变负荷的患者制作个体化疫苗。
此外,个体化新抗原癌症疫苗很可能会面临严酷的市场竞争。各种针对癌细胞的融合蛋白取得较好的临床效果,如T细胞衔接器和双特异性抗体,以及肿瘤浸润性淋巴细胞治疗的商业化等。
3.3 机:联合用药有望为癌症治疗带来新的突破
抗肿瘤免疫反应最重要的目标是用记忆T细胞持久地对抗癌细胞。在这方面,肿瘤新抗原的特异性免疫治疗是最合理的方法之一,值得进一步探索。比如,癌症靶向疫苗与ICIs的联用,以增强对癌细胞的免疫应答。此外,为了打破免疫耐受,各种重塑肿瘤微环境的手段也应与个体化癌症疫苗治疗相结合。
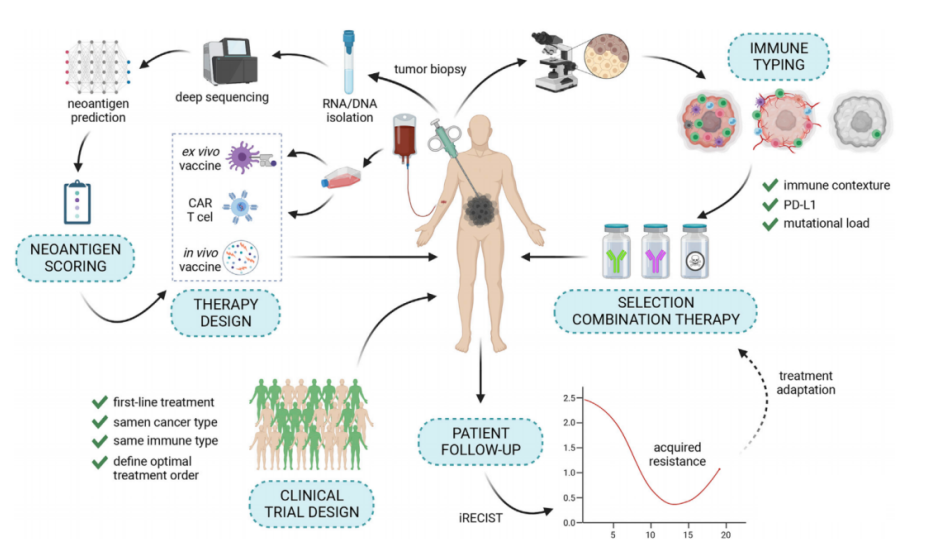
ICIs的确显著提高了生存率,但有部分转移性黑色素瘤患者对ICIs治疗无反应或不耐受,这表明ICIs治疗下仍然存在未满足的临床需求。如此,个性化的癌症靶向免疫疗法应该是下一代治疗的发展方向。
技术的整合和优化是个体化新抗原癌症疫苗研发的关键,相信随着技术的不断进步,如下一代测序技术、人工智能算法和合成生物学等的发展,个体化新抗原癌症疫苗的研究和应用将会不断取得新的突破。同时,临床试验的开展也将为其安全性和有效性提供更多的数据支持。
参考资料:
1.Terai M, Sato T. Individualised neoantigen cancer vaccine therapy. Lancet. 2024;403(10427): 590-591.
2.Laucius JF, Bodurtha AJ, Mastrangelo JM, Bellet RE. A phase II study of autologous irradiated tumor cells plus BCG in patients with metastatic malignant melanoma. Cancer 1977; 40: 2091–93.
3.Weber, Jeffrey S et al. “Individualised neoantigen therapy mRNA-4157 (V940) plus pembrolizumab versus pembrolizumab monotherapy in resected melanoma (KEYNOTE-942): a randomised, phase 2b study.” Lancet (London, England) vol. 403, 10427 (2024): 632-644.
4.Sahin, U., & Türeci, Ö. (2018). Personalized vaccines for cancer immunotherapy. Science (New York, N.Y.), 359(6382), 1355–1360.
5.https://www.modernatx.com/en-AU
本篇文章来源于微信公众号: 求实药社