- A+
"
近日,纪念斯隆-凯特琳癌症中心(MSKCC)的精准肿瘤学数据库(OncoKB)获得了美国FDA的部分认可,它是第一个被FDA部分认可的癌症体细胞变异数据库,以后肿瘤基因检测公司可以使用这些数据来支持上市前提交的肿瘤分析测试的临床有效性。
FDA为监管基于NGS的检测创建了一个灵活和适应性的监管方法,其于2018年4月发布的“使用公共人类遗传变异数据库支持基于遗传和基因组的体外诊断的临床有效性”指南为NGS检测公司提供了一种机制,可以使用FDA认可的公共人类遗传变异数据库来支持FDA对遗传和基因组检测的监管审查。1 使用FDA认可的数据库将为NGS检测公司提供一条有效的途径来获得NGS新检测产品的市场许可或上市批准。
这也就意味着NGS检测公司不必独立证明用于验证其单个检测的数据库的合法性,而是可以使用FDA认可的数据库来支持他们的检测验证。
2018年12月4日,FDA认可临床基因组资源联盟的ClinGen数据库,这是首个被纳入公共人类遗传变异数据库的基因变异数据库,也是首个遗传病突变数据库(胚系突变)。2
截至2021年10月,FDA还没有认可第二个基因变异数据库,尤其是针对体细胞突变的数据库。
2021年10月7日,FDA批准将MSKCC的OncoKB部分数据库列为第一个被纳入公共人类遗传变异数据库的肿瘤突变数据库,这是FDA认可第二个基因变异数据库,也是首个肿瘤突变数据库(体系突变)。3
▲ FDA认可的首个肿瘤突变数据库

▲ 截至目前,FDA已认可的数据库列表
OncoKB,是纪念斯隆-凯特琳癌症中心(MSKCC)的研究人员和临床医生共同开发的精准肿瘤学知识数据库,包含125个癌种相关的682个癌症基因的特定变异详细信息(包括治疗、诊断和预后),这些数据来源包括FDA、NCCN、ASCO、AACR或ESMO会议论文及其他公共癌症变异数据库等。每条信息均经过临床基因组学注释委员会(CGAC)的定期审阅与修订。
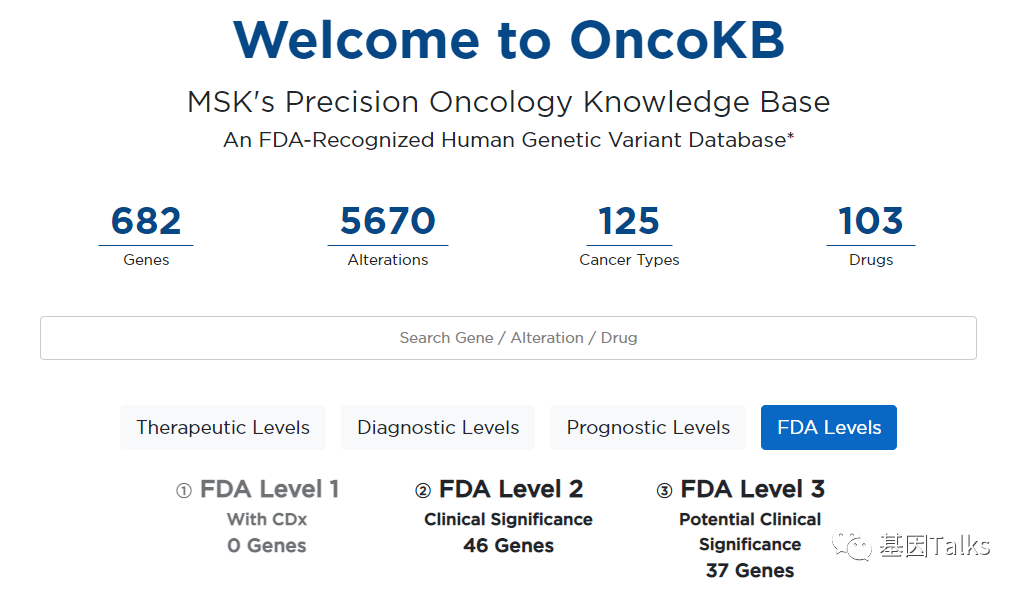
▲ https://www.oncokb.org
2021年10月7日,OncoKB数据库获得了美国FDA的部分认可,它是第一个被FDA部分认可的癌症体细胞变异数据库(体系变异是生命后期发生的改变,而不是出生时遗传的胚系变异)。
FDA认可OncoKB数据库中一部分为2级(临床意义,46个基因)和3级(潜在临床意义,37个基因)共83个基因生物标志物(注意,FDA 2级和3级的基因有重叠部分,整合后为66个基因)的有效科学证据来源,可用于简化肿瘤NGS分析测试的开发和验证过程。以后肿瘤基因检测公司可以使用这些数据来支持上市前提交的肿瘤分析测试的临床有效性。使用DNA测序确定肿瘤的突变谱进而指导靶向治疗和研究性治疗方案。
由于OncoKB不包含针对特定治疗产品的任何CDx声明,因此根据定义,OncoKB中的任何基因变异都不会被视为FDA 1级。

▲ FDA认可的证据级别,其中1级为CDx;2级为具有临床意义的突变:使医疗保健专业人员根据临床证据(如专业指南中提出的临床证据)使用有关患者肿瘤的信息。这类信息得到了分析有效性(适当情况下针对突变本身或通过代表性的方法)和临床有效性(通常基于公开的临床证据,如专业指南和/或同行评审的出版物)的证据支持;3级为具有潜在临床意义的突变:不被认为是1级或2级生物标志物的突变可以被描述为具有潜在临床意义的癌症突变。这些突变可能可以提供有用的信息,或用于指导患者参加可能适合于他们的临床试验。此类信息得到了分析有效性(适当情况下通过代表性方法)和纳入专家组临床或基础机制(通常包括同行评审的出版物或体外临床前研究模型)的证据支持。
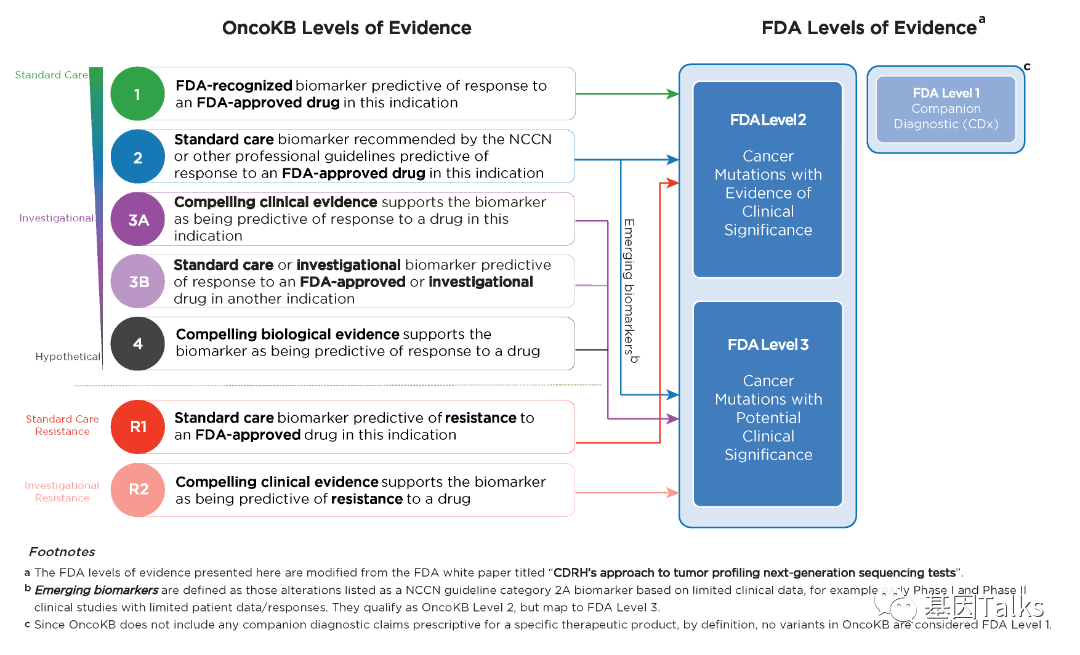
▲ OncoKB证据级别与FDA证据级别之间的映射:由于OncoKB不包括诊断公司要求处方针对特定治疗产品的任何CDx声明,因此根据定义,OncoKB中的任何基因变异都不会被视为FDA 1级;OncoKB的1类和2类证据,以及标准耐药性变异R1证据均映射到FDA 2级;OncoKB的2类新兴生物标志物(NCCN中的2A类)和3A,3B和4类证据,以及临床试验支持的耐药性变异R2证据均映射到FDA 3级。
更为直观的分类如下:FDA药物标签和部分NCCN指南为FDA 2级(临床意义),部分NCCN指南和同行评审的出版物以及OncoKB评估的基于生物标志物的研究或分析类型为FDA 3级(潜在临床意义)。
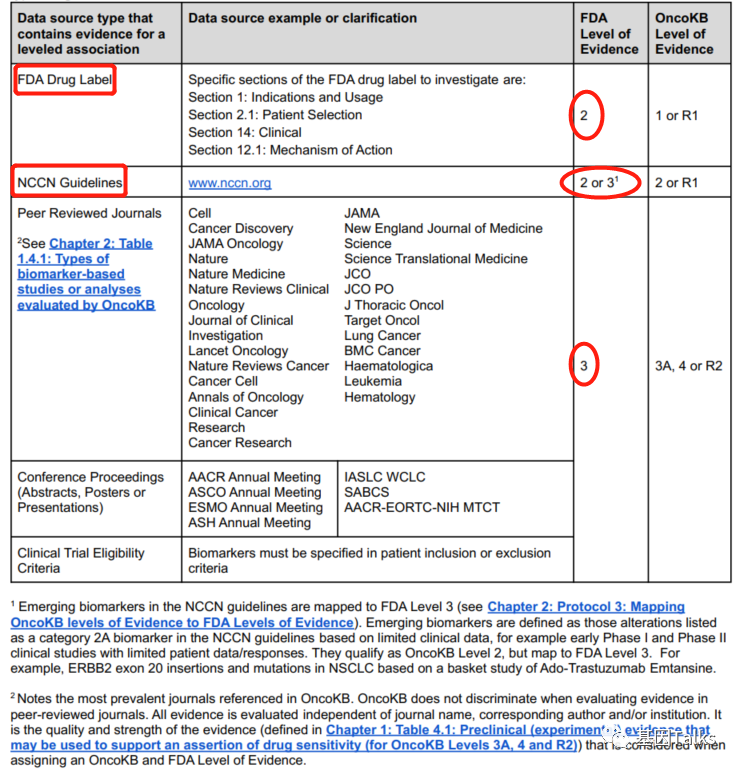
具体FDA认可的OncoKB基因信息,可以去OncoKB官网进行查询,包括基因,变异位点,癌症类型及FDA 证据等级信息。4
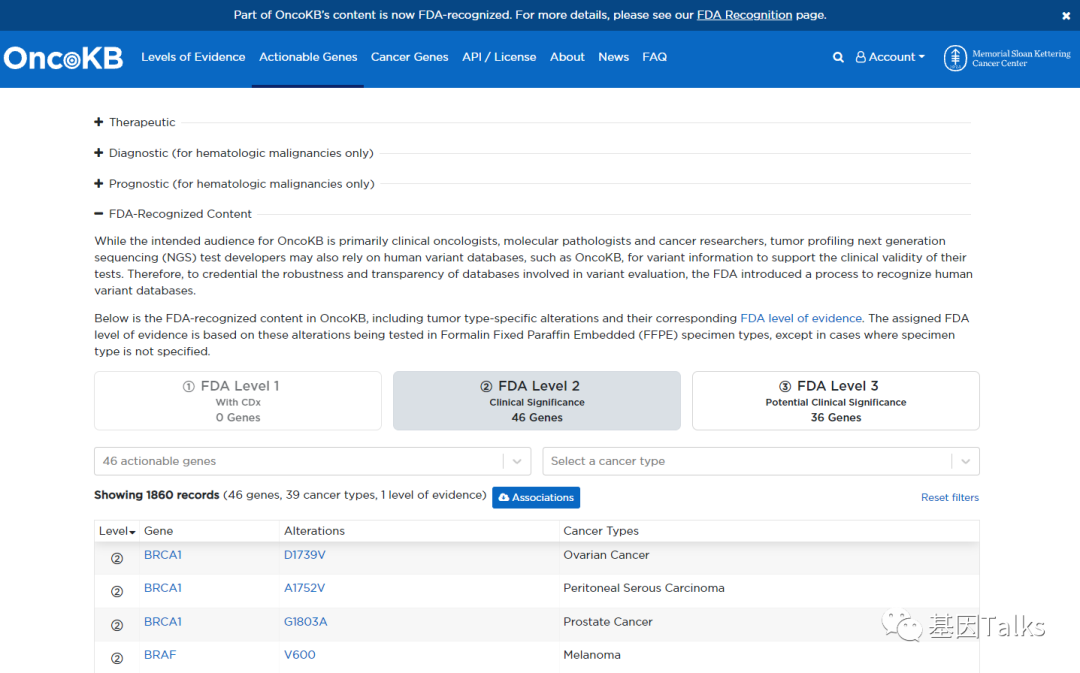
*注意,FDA 3级基因在详细列表与首页略有差异,一个显示36基因,一个显示37基因,可能刚批准还没更新完善。
1)什么是OncoKB?
OncoKB ( https://www.oncokb.org ) 是一个精准肿瘤学知识数据库,用于注释癌症基因变异的生物学结果和临床意义(包括治疗、诊断和预后)。
2)OncoKB是否同时管理体系和胚系变异?
目前,OncoKB的重点是癌症治疗中的体系变异。但是,MSKCC的研究人员和临床医生也在计划扩展OncoKB数据库以包括胚系变异的注释。
3)OncoKB和 cBioPortal 之间有什么区别?
癌症基因组学的cBioPortal拥有癌症基因组学数据,包括来自已发表的测序工作(如TCGA)的患者遗传变异。OncoKB包含关于癌症中特定基因改变的手工整理信息,并提供了一个用于注释患者变异的API(尽管OncoKB本身不包含来自患者的任何数据)。例如,cBioPortal利用OncoKB API在这个数据库中注释癌症变异。换句话说,cBioPortal包含关于在单个肿瘤样本中观察到哪些突变的信息(通过聚合来自多个患者的数据,cBioPortal包含关于基因和变异改变频率的信息),而OncoKB包含关于变异的影响和治疗意义的信息。两者都可以组合在一起,但来自OncoKB的信息也可以应用于不在cBioPortal中的任何其他数据集。
4)我们应如何引用OncoKB?
使用OncoKB时,需引用:Chakravarty et al., JCO PO 2017.
5)OncoKB 是医疗产品吗?
不,OncoKB 不是医疗产品。
6)FDA对OncoKB的认可涉及哪些方面?
OncoKB于2018年8月开始寻求FDA认可,并于2021年10 月7日获得部分认可。FDA对人类变异数据库的认可涉及FDA对数据库标准操作程序(SOP)和政策的详细审查,包括流程和验证研究用于变体评估和管理、数据完整性和安全性以及所有证据的透明度。FDA还审查了数据库管理政策,以招聘、培训和继续教育策划、评估和批准将变体纳入数据库的人员,以及确保他们的利益冲突最小化和透明的流程。
7)OncoKB 提供临床试验匹配吗?
目前可根据OncoKB注释的药物和患者癌症类型进行匹配临床试验。MSKCC将通过OncoKB的 API 提供匹配的临床试验。
参考资料:
1.https://www.fda.gov/media/99200/download
2.https://www.fda.gov/news-events/press-announcements/fda-takes-new-action-advance-development-reliable-and-beneficial-genetic-tests-can-improve-patient
3.https://www.fda.gov/drugs/resources-information-approved-drugs/fda-recognizes-memorial-sloan-kettering-database-molecular-tumor-marker-information
4.https://www.oncokb.org/actionableGenes#levels=FDAx2§ions=FDA
本篇文章来源于微信公众号: 基因Talks